Blog
Titulação: Término da análise de proteína Kjeldahl
titulação,análise,proteína,kjeldahl
A titulação é uma das técnicas mais utilizadas nos laboratórios, entretanto, alguns detalhes garantem sua eficiência, sendo capazes de evitar erros na determinação da concentração de proteína na amostra.
A titulação é a última etapa da análise de proteína pelo método Kjeldahl, e ocorre após a amostragem e preparo da amostra.
O método de determinação de nitrogênio total foi desenvolvido há mais de 130 anos pelo dinamarquês Johan Gustav Kjeldahl, e desde então, tem sido estudado, modificado e melhorado. O método Kjeldahl é referência ou padrão para quantificar o teor de proteína em alimentos, sendo recomendado por órgãos normalizadores como AOAC e ISO. Esse método quantifica o teor de nitrogênio total e estima indiretamente o teor de proteína dos alimentos.
Método Kjeldahl
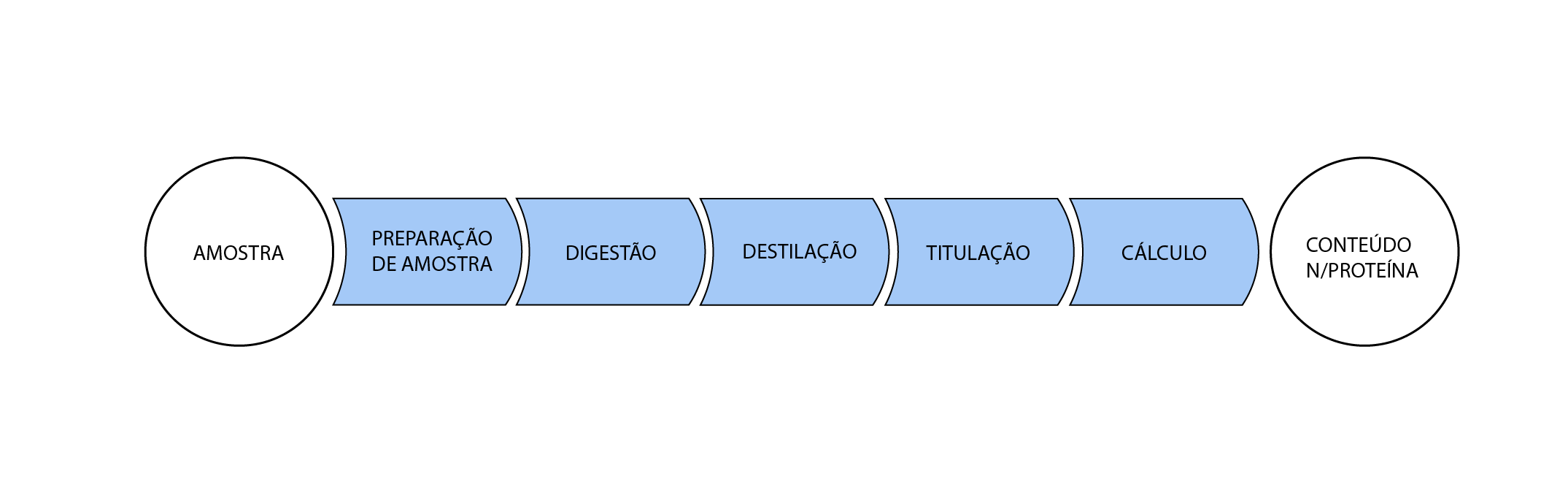
O método consiste na digestão com ácido sulfúrico concentrado e uma mistura catalítica para acelerar a reação, seguida de destilação com hidróxido de sódio para liberação do íon amônio que é retido em ácido bórico.
A última etapa é a titulação com ácido forte padronizado para quantificação do nitrogênio total presente na amostra. O teor de proteína é então estimado indiretamente através de cálculo, multiplicando o teor de nitrogênio por um fator de conversão.
O resultado final da análise, ou seja, o teor de proteína, é dependente da qualidade de cada etapa do processo analítico.
Titulação
A titulação é uma análise química quantitativa utilizada para determinar a concentração de uma substancia em uma amostra. O princípio básico da titulação é adicionar uma solução titulante ou padrão, de concentração conhecida, na solução a ser analisada.
A solução titulante é adicionada lentamente com o auxílio de uma bureta digital, modelo hirschmann, até que a reação atinja a neutralização, geralmente indicada por uma mudança de cor. Os tituladores potenciométricos modelos, KEM-AT-710 ou KEM-AT-710S podem ser utilizados no lugar da bureta.
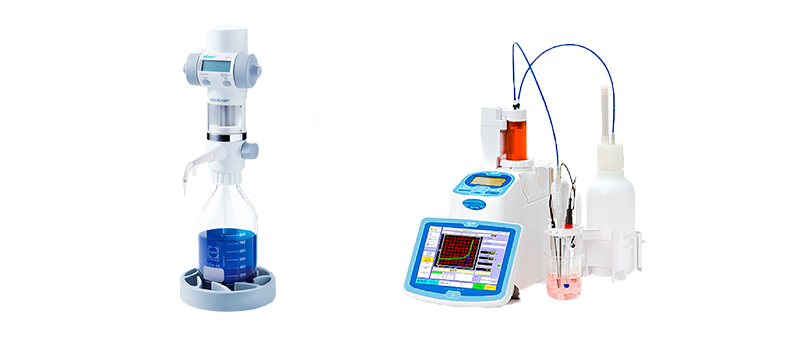
Na análise de proteína, o destilado obtido na etapa anterior é submetido a titulação. A amônia é titulada diretamente pelo ácido clorídrico padronizado (HCl 0,1 mol/L) que desloca da molécula de borato, separando o borato de amônio formado na destilação.
O volume de solução titulante requerido para amostra e para amostra em branco, juntamente com o fator de correção do ácido clorídrico e o fator de conversão de nitrogênio são utilizados para o cálculo final para obter a concentração de proteína na amostra (cálculo disponível no final da página). O fator de conversão de nitrogênio varia em função do tipo de produto, mas de modo geral o valor de 6,25 é aplicado para diversas amostras.
Embora todas as etapas da análise de proteína devam ser executadas de maneira criteriosa, a não padronização ou padronização incorreta do ácido clorídrico é a maior fonte de erros na etapa de titulação. Além disso, a definição do ponto de parada da titulação também prejudica o resultado da análise.
Padronização do ácido
A padronização de soluções desempenha um papel fundamental nos métodos titulométricos de análise. Em uma padronização, a concentração de uma solução volumétrica é determinada pela sua titulação contra uma quantidade cuidadosamente medida de um padrão primário, secundário ou do volume exatamente conhecido de outra solução padrão.
Esse procedimento é muito comum em laboratório para definir a concentração exata de uma solução preparada com um constituinte (soluto) que é volátil, higroscópico ou não possui alto grau de pureza.
A não padronização ou padronização incorreta do Ácido clorídrico, pode comprometer todas as etapas anteriores (amostragem, digestão, destilação), pois não garante a real concentração do titulante, prejudicando o cálculo da concentração de nitrogênio. Confira, no final da página como realizar a padronização do ácido.
Ponto final da titulação
O ponto final da reação é determinado pela verificação da alteração de uma propriedade física, como a cor, para tentar determinar o ponto de equivalência. Este ponto pode ser determinado por meio visual, com uso de indicadores.
Os indicadores não mudam de cor
instantaneamente. No caso da titulação ácido-base, o indicador pode ficar
inicialmente com coloração mais clara antes de mudar completamente. Na análise de proteína, a solução destilada é
titulada com ácido clorídrico 0,1 mol/L padronizado, até o aparecimento da coloração
levemente avermelhada e persistente, conforme figura abaixo.
Cada analista pode perceber as cores de maneira diferente, o que pode afetar a precisão e repetibilidade do resultado. Se a cor se altera pouco, grande quantidade do titulante é adicionado, prejudicando os resultados finais. Dessa forma, a experiência e percepção do analista contribuem na padronização dos resultados.

Considerações finais
O erro laboratorial é qualquer falha ocorrida em qualquer parte do processo de análise. Dessa forma, um laboratório de análise precisa ter um controle de qualidade que possibilite verificar se os procedimentos estão sendo conduzidos de maneira correta.
A elaboração de uma relação contento os principais erros e como cada um pode afetar o resultado, é uma ferramenta útil para ser utilizada.
Além disso, é de extrema importância que os procedimentos sejam executados por equipe treinada e capacitada, pois a falta de preparo é considerada um interferente, não somente para análise de proteína, como para os demais processos.
É importante que os equipamentos utilizados estejam em perfeitas condições e as vidrarias utilizadas devem ser calibradas.
O processo de amostragem, incluindo a coleta de amostra, quarteamento, homogeneização e moagem são tão importantes como as etapas de digestão, destilação e titulação.
No preparo das soluções e desenvolvimento da marcha analítica, deve ser utilizado água de boa qualidade, pois ela também é considerada um interferente. Saiba mais no conteúdo sobre "Tipos de água utilizados no laboratório e principais aplicações".
1) Solução volumétrica padronizada de Ácido
clorídrico 0,1 mol/L
Medir 8,5 mL de Ácido clorídrico e transferir para balão volumétrico de 1000 mL, contendo aproximadamente 500 mL de água. Esfriar, completar o volume e homogeneizar.
Padronização:
pesar em Erlenmeyer aproximadamente 0,133 g de carbonato de sódio, previamente seco
a 105 °C por 2 horas. Dissolver em 50 mL água. Adicionar 3 gotas de solução de vermelho
de metila 0,1% (m/v). Titular até viragem para coloração rósea. Aquecer a
ebulição, para eliminar o gás carbônico. Se a coloração rósea não for
persistente, esfriar e prosseguir a titulação. O ponto exato de viragem da
solução de ácido clorídrico 0,1 mol/L ocorre em pH 4,4.
Cálculo da molaridade real:
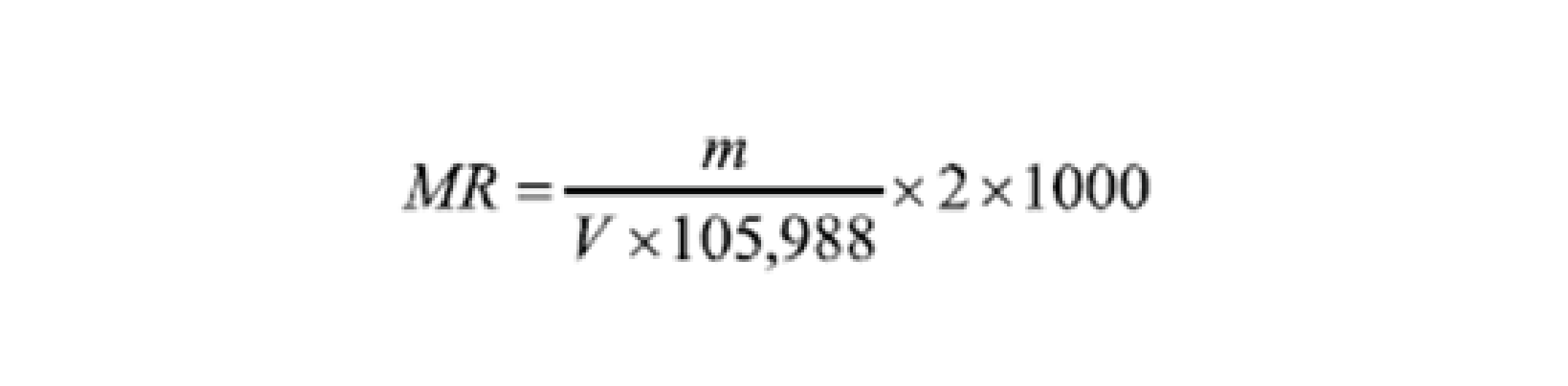
Onde:
MR: Molaridade real da solução de ácido clorídrico 0,1
mol/L
M: Massa do carbonato de sódio, em g
105,988: Massa molar do carbonato de sódio
V: Volume da solução de ácido clorídrico 0,1 mol/L gasto na titulação, em mL
2 / 1: Relação estequiométrica entre ácido clorídrico
e carbonato de sódio
1000:
Conversão entre unidades de volume (mL e L)
2) Cálculo final
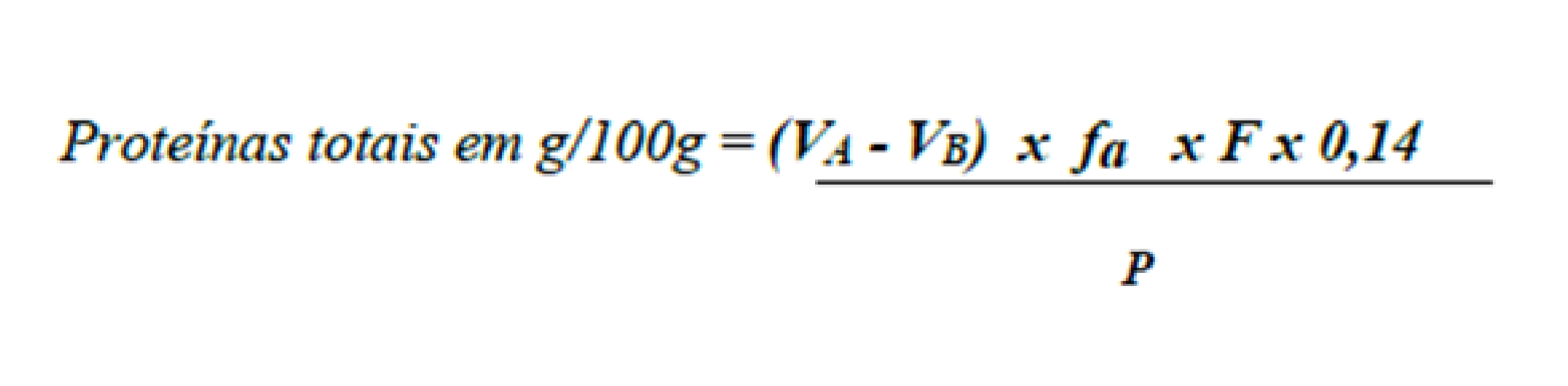
Onde:
VA = volume de Ácido clorídrico 0,1 mol/L padronizado
gasto na titulação da amostra.
VB = volume de Ácido clorídrico 0,1 mol/L padronizado
gasto na titulação do branco.
fa = fator de correção da solução de Ácido clorídrico
0,1 mol/L.
F = fator de conversão de nitrogênio para proteína. Na maioria dos alimentos, calcula-se que o nitrogênio representa aproximadamente 16% do peso da proteína, assim, em 100g de proteína tem-se 16g de nitrogênio, e 100/16= 6,25, que corresponde ao fator de conversão de nitrogênio para proteína. Abaixo, algumas sugestões de fatores de conversão:

Quer saber mais, baixe o e-book exclusivo.
Sobre a Tecnal
A Tecnal tem como missão contribuir para o desenvolvimento científico, tecnológico e com a indústria nacional e internacional por meio da fabricação e da comercialização de equipamentos científicos, da prestação serviços especializados e da disseminação do conhecimento. A empresa busca crescer de maneira inovadora e sustentável, focada na continuidade e na excelência operacional, de forma a tornar-se uma referência no mercado brasileiro e internacional de equipamentos científicos. Fale conosco: Telefone/WhatsApp (19) 2105-6161, e-mail: contato@tecnal.com.br ou pelo nosso site clicando aqui.
Referências
IAL, Instituto Adolfo Lutz. Métodos físico-químicos para análise de alimentos. São Paulo: Instituto Adolfo Lutz, p. 1020, 2008.
LOCATELLI, Tamiris. Determinação de proteínas em suplementos alimentares. Revista Cientifica Multidisciplinar Núcleo do Conhecimento. Ano 03, Ed 08, Vol. 03, pp 21-47, Agosto 2018. ISSN:2448-0959.
SINDIRAÇÕES, Sindicato Nacional da Indústria de Alimentação Animal. Compêndio Brasileiro de Alimentação Animal. Guia de métodos analíticos. 2017.
